
Por Martha A. Lomelí P.
La cristalización es un proceso fundamental en la ciencia de los materiales y la química, que se refiere a la formación de cristales a partir de una solución, fundido o vapor. Este fenómeno no solo es clave en la fabricación de productos químicos y farmacéuticos, sino que también tiene aplicaciones en la geología, la metalurgia, la biología, etcétera.
Durante la cristalización, las partículas presentes en una solución o un líquido se organizan en una estructura ordenada y repetitiva, formando un sólido cristalino. Este proceso puede verse influenciado por diversos factores, como la temperatura, la concentración del soluto y la presencia de impurezas. Además, la forma y las propiedades de los cristales resultantes pueden variar significativamente dependiendo de las condiciones bajo las cuales se lleva a cabo la cristalización.
Comprender este proceso es esencial para optimizar la producción de sustancias puras y mejorar la calidad de los productos finales. En resumen, la cristalización no solo es un fenómeno fascinante desde el punto de vista científico, sino que también tiene un impacto práctico significativo en diversas industrias.
Métodos de cristalización
Existen diferentes métodos para formar cristales, entre ellos:
1. Por evaporación
Consiste en disolver un soluto en un solvente y luego evaporar controladamente el solvente. A medida que la concentración del soluto aumenta, comienzan a formarse cristales. Es un método sencillo y eficaz para compuestos solubles.
2. Por enfriamiento
Se disuelve un soluto en un solvente caliente y, al enfriar lentamente la solución, la solubilidad del soluto disminuye, favoreciendo la formación de cristales. Es común en la purificación de compuestos químicos.
3. Por supersaturación
Implica crear una solución donde la concentración del soluto es mayor que su solubilidad en condiciones normales, lo que puede lograrse enfriando una solución caliente o evaporando el solvente. Agitar o introducir un cristal semilla favorece la nucleación.
4. Por filtración
Se utiliza para recuperar los cristales formados en una solución, separándolos mediante filtración.
5. En frío
A bajas temperaturas, la solubilidad de ciertos compuestos disminuye, facilitando la cristalización.
6. En solución
El soluto se disuelve en un solvente adecuado y se permite la formación de cristales directamente en la solución. Es útil para compuestos difíciles de cristalizar.
7. Por sublimación
En este proceso, un sólido se convierte directamente en vapor y luego se condensa en una superficie fría. Es ideal para compuestos que subliman.
8. Métodos de enfriamiento controlado
Se regula cuidadosamente la tasa de enfriamiento para influir en la morfología y la pureza de los cristales.
Cada método tiene sus ventajas y desventajas, y la elección depende del tipo de sustancia, la pureza deseada y las condiciones experimentales.
¿Te gustaría hacer tus propios cristales?
Necesitarás:
– Sal de mesa
– Recipiente
– Agua
– Limpiapipas
– Cuchara
– Alambre o abatelenguas para sujetar el limpiapipas

Primero, la cantidad de agua y sal dependerá del tamaño del objeto donde crecerán los cristales (limpiapipas), pero debe superar los 359 g de sal por litro de agua. Agrega la sal poco a poco al agua. Cuando la sal ya no se disuelva, habrás alcanzado el límite de solubilidad. Para disolver más, será necesario calentar el agua, sin superar los 400 g por litro.


Coloca el recipiente en un sitio donde no se mueva en los próximos días.
Ahora deja volar tu imaginación: dobla el limpiapipas en la figura que prefieras (un corazón, una estrella, un copo de nieve, etc.) y colócalo dentro de la solución usando el alambre o abatelenguas como soporte.



Después de varios días, notarás cómo los cristales comienzan a crecer entre las hebras del limpiapipas. Cuando tengan el tamaño deseado, retíralo con cuidado y déjalo secar al sol.
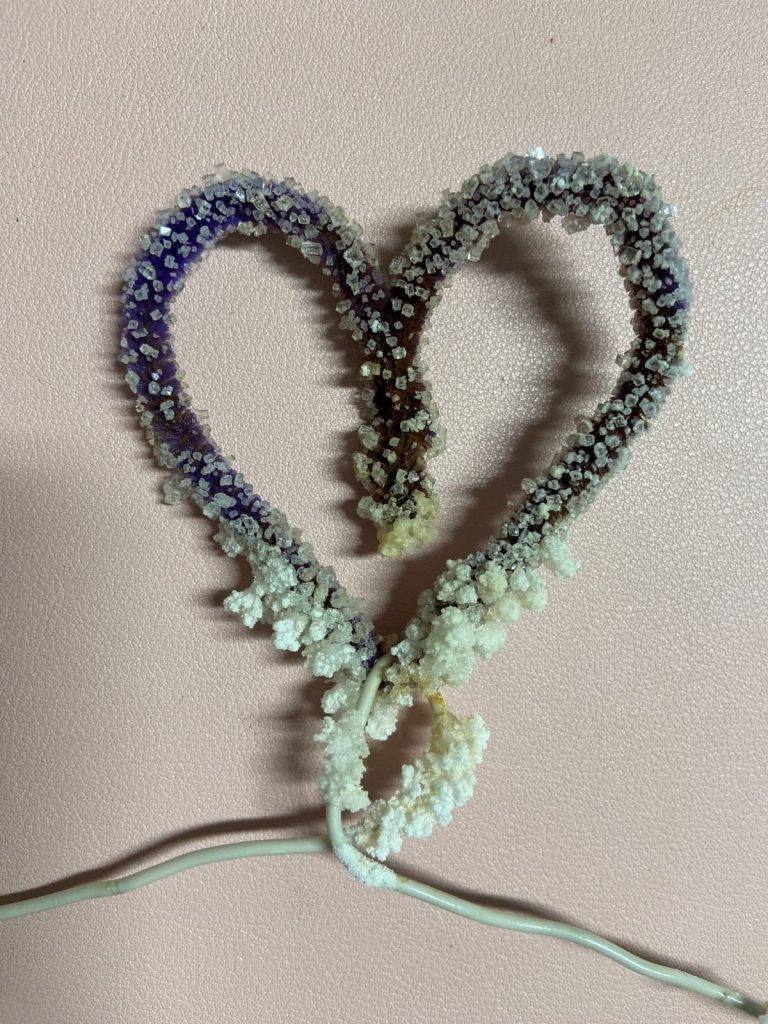

¿Te gustó el experimento? ¿Qué método de cristalización utilizamos en este experimento? ¿Qué forma tienen los cristales que se formaron?
Puedes intentar algo más, recorta un cartón con forma de árbol de Navidad, colócalo armado en un plato hondo, pero poco profundo, vierte la solución salina y observa cómo, en pocos días, crece un árbol de cristales. Solo asegúrate de que el cartón sea lo suficientemente resistente. Y el resultado será similar que los kits que encuentras a la venta.
¿Sabías que todos los copos de nieve son cristales?
Aunque comparten una estructura hexagonal debido a cómo se unen las moléculas de agua al congelarse, no hay dos copos de nieve iguales. Las condiciones de temperatura y humedad hacen que cada cristal crezca de forma única. ¡La cristalización natural crea verdaderas obras de arte irrepetibles!





